Marches pour les Sciences

Le 22 avril, auront lieu dans le monde entier, des « Marches pour les sciences ».
La Société des Neurosciences, comme la FENS et de nombreuses sociétés scientifiques internationales, s’associe à cette action qui a pour objectif de mettre en avant l’importance pour le bien commun et la civilisation de la démarche scientifique, respectant les faits et l’honnêteté intellectuelle, ouverte à tous dans le monde entier.
Pour plus d’information sur les actions en France :
un anxiolytique naturellement efficace !

Des chercheurs de l’Institut des maladies neurodégénératives de Bordeaux (IMN-UMR-CNRS 5293 / Université de Bordeaux) viennent de découvrir que les réactions anxieuses occasionnées par des facteurs de stress pourraient être le reflet des changements synaptiques qui s’opèrent dans une petite région du cerveau : Le noyau du lit de la strie terminale (BNST). A travers des expériences conduites chez des rats exposés à des situations anxiogènes, les chercheurs ont disséqué un circuit neuronal qui, lorsqu’il est activé, réduit les niveaux d’anxiété de l’animal pendant plusieurs jours. Ces résultats, issus d’une collaboration entre deux laboratoires bordelais (IMN-UMR-CNRS 5293 et INCIA-UMR-CNRS 5287) et un laboratoire suisse (FMI, Basel, Switzerland) sont publiés dans Nature Communications, le 20 Février 2017.
L’anxiété est une émotion physiologique qui déclenche un état d’alerte en réponse à une menace réelle ou supposée et constitue ainsi un mécanisme de survie. Le noyau du lit de la stria terminalis (BNST) appartient à un réseau neuronal de régions limbiques interconnectées et exerce un rôle central dans l’expression de l’anxiété chez de nombreuses espèces animales, et notamment chez l’Homme. Les auteurs de l’étude ont utilisé des approches virales pour tracer les voies neuronales dans trois régions cérébrales impliquées dans les comportements associés à l’état d’anxiété. Ils ont enregistré et manipulé, in vivo, l’activité électrique des neurones. Ils ont ainsi mis en évidence qu’une population de neurones du BNST (centre cérébral de la motivation et de l’anxiété), intégrait et filtrait des informations en provenance du subiculum ventral (centre cérébral de la mémoire des émotions) et du cortex infralimbique (centre cérébral de la mémoire et des habitudes) pour augmenter de façon persistante leur activité. Les conséquences de ce changement d’état des neurones du BNST sont, en particulier des changements d’état anxieux de l’animal.
Les chercheurs ont ainsi pu déterminer que la mise en place d’une plasticité de type potentialisation à long terme au niveau des synapses « subiculum ventral/BNST » provoque un effet activateur et persistant (plusieurs jours) sur les neurones du BNST ayant pour conséquence de jouer le rôle d’un anxiolytique.
Ce travail, en précisant les circuits neuronaux et mécanismes de plasticité synaptique qui réduisent les niveaux d’anxiété de l’animal de manière persistante, ouvre de nouvelles perspectives pour comprendre comment un changement de l’état synaptique des neurones du BNST pourrait modifier la perception de stimuli sensoriels en condition pathologique (addiction, trouble de l’anxiété). Ces travaux ont été financés notamment par l’Agence nationale pour la recherche (ANR), le CNRS et l’université de Bordeaux.
Référence:
NMDA-receptor-dependent plasticity in the bed nucleus of the stria terminalis triggers long-term anxiolysis.Glangetas C, Massi L, Fois GR, Jalabert M, Girard D, Diana M, Yonehara K, Roska B, Xu C, Lüthi A, Caille S, Georges F. Nat Commun. 2017 Feb 20;8:14456.
Contact auteur : Dr François GEORGES, CNRS/Université de Bordeaux : francois.georges@u-bordeaux.fr / Tel : +33 5 33 51 48 13
Hightlights NeuroFrance 2017

NeuroFrance 2017, un programme plus dense, plus riche :
7 conférenciers pléniers de renommée internationale, 42 symposiums, des symposiums spécialisés, des sessions « Réussir avec une thèse en neurosciences », lectures de CV et courts entretiens, près de 600 posters
Une exposition commerciale de plus de 45 stands
NeuroNight : pour une soirée mémorable en bord de Garonne !
Ne ratez pas l’occasion de participer et de découvrir Bordeaux, numéro 1 des villes à visiter en 2017 selon le Lonely Planet !
Inscrivez-vous avant le 5 avril pour bénéficier des tarifs préférentiels !
Faits marquants 2016

Pour élaborer ces « faits marquants 2016 », les membres du Conseil d’Administration de la Société des Neurosciences ont sélectionné quelques publications parmi les plus remarquables dans leur discipline. Les magnifiques découvertes présentées ici témoignent de la vitalité des Neurosciences françaises, et de la réalité de l’avancement des connaissances dans toutes les branches des Neurosciences, grâce aux chercheurs en France. Bien d’autres articles auraient mérité d’être dans cet échantillon !

Consultez les faits marquants 2016
La huntingtine, une protéine essentielle à l’assemblage du cortex cérébral

Le cortex des mammifères est formé de six couches de neurones dont l’assemblage est précisément régulé au cours du développement. Les neurones excitateurs corticaux (également appelés neurones de projection) sont produits dans la zone ventriculaire, subissent ensuite une transition multipolaire-bipolaire, une migration radiale et une différenciation. Nous montrons dans cette étude que la huntingtine (HTT), protéine mutée dans la maladie de Huntington (MH), est nécessaire pour la transition multipolaire-bipolaire des neurones de projection et pour le maintien de leur forme bipolaire lors de leur migration radiale. La HTT est responsable de ces effets in vivo en agissant sur le trafic de la N-Cadhérine qui dépend de la petite protéine GTPase RAB11. Lorsque la HTT contient la mutation responsable de la MH ces mécanismes sont altérés. Enfin, nous montrons que les défauts corticaux résultant de la perte post mitotique de la HTT spécifiquement pendant le développement embryonnaire affectent la morphologie neuronale à l’âge adulte.
Ces travaux sont importants pour plusieurs raisons. Alors que la MH est une maladie neurologique héréditaire se manifestant à l’âge adulte, il y a de plus en plus d’évidences qu’un développement anormal contribuerait aux symptômes observés à l’âge adulte. Nos travaux vont dans ce sens en établissant une nouvelle fonction de la HTT au cours du développement cortical, fonction qui est altérée dans la MH. De façon plus générale, notre étude souligne précisément comment la transition multipolaire-bipolaire des neurones de projections qui a lieu pendant la période embryonnaire influence la position des neurones mais également leur morphologie.
Référence de l’article: Barnat M, Le Friec J, Benstaali C, Humbert S. Huntingtin-mediated Multipolar-Bipolar Transition of Newborn Cortical Neurons is Critical for their Postnatal Neuronal Morphology, Neuron. 2017 Jan 4;93(1):99-114. doi: 10.1016/j.neuron.2016.11.035.
Contact: Sandrine Humbert, INSERM, U1216, Univ. Grenoble Alpes, Grenoble Institut des Neurosciences, GIN, Grenoble, France.
Crédit photo : M. Barnat
La Testostérone pour Réparer la Myéline
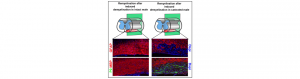
Dans le système nerveux central, les gaines de myéline qui protègent les axones et contribuent à la rapidité de la conduction nerveuse sont produites par les oligodendrocytes. Lors de pathologies démyélinisantes, la myéline détruite peut être spontanément régénérée par un processus appelé remyélinisation. En utilisant un modèle murin de démyélinisation focale de la moelle épinière, une étude récente co-dirigée par le Dr. Michael Schumacher et le Dr. Elisabeth Traiffort (INSERM U1196, Université de Paris-Sud, Université Paris-Saclay) vient de rapporter un rôle clé des gonades mâles, de la testostérone et du récepteur des androgènes dans ce processus régénératif. L’absence de l’hormone sexuelle mâle ou de son récepteur empêche le recrutement des astrocytes au sein de la région démyélinisée et de façon concomitante, prévient la différenciation des progéniteurs oligodendrocytaires en oligodendrocytes matures capables de synthétiser la myéline présente dans le système nerveux central. A la place de cette myéline contenant notamment les deux protéines majeures que sont la protéine basique de la myéline (MBP) et la protéine protéolipidique (PLP), les chercheurs observent la production d’une myéline classiquement synthétisée par les cellules de Schwann dans le système nerveux périphérique et qui est majoritairement composée de la protéine zéro (P0) et de la protéine périphérique de la myéline (PMP22). Ce lien étroit entre la testostérone et la production de myéline pourrait trouver son origine dans l’évolution des espèces animales puisque l’on constate que le récepteur des androgènes est apparu tardivement et en même temps que la myéline chez les vertébrés dotés d’une mâchoire. Ces travaux, publiés récemment dans le journal PNAS, peuvent contribuer à expliquer l’évolution différente des maladies démyélinisantes telles que la sclérose en plaques chez les femmes et chez les hommes et pourraient avoir des implications importantes dans le contexte des désordres psychiatriques ou des pathologies cognitives liées au vieillissement.
Bielecki B, Mattern C, Ghoumari AM, Javaid S, Smietanka K, Abi Ghanem C, Mhaouty-Kodja S, Ghandour MS, Baulieu EE, Franklin RJ, Schumacher M*, Traiffort E*.
(*Co-last authors).
Unexpected central role of the androgen receptor in the spontaneous regeneration of myelin.
Proc Natl Acad Sci U S A click to read. 2016 Dec 20. doi: 10.1073/pnas.1614826113.
Nouvelle méthode de marquage de protéines pour la microscopie super-résolution
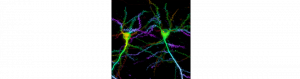
de Olivier Thoumine
Afin de cartographier la dynamique et l’organisation à l’échelle nanométrique des complexes d’adhérence synaptique, nous avons développé une stratégie polyvalente basée sur des monomères de streptavidine (~3 nm) conjugués à des fluorophores organiques robustes. Ces nanosondes ciblent des protéines membranaires sélectivement biotinylées sur une petite étiquette positionnée au niveau de leur domaine extracellulaire. L’approche est très spécifique, et permet un marquage efficace dans des environnements cellulaires confinés avec un encombrement stérique réduit et aucun biais de réticulation par rapport à des sondes multivalentes. Cette stratégie est compatible avec la plupart des techniques de super-résolution (STORM, STED et PAINT), et en mode multi-spectral.
L’article a bénéficié d’un research highlight dans Nature Methods et s’accompagne d’un protocole à paraître prochainement dans Nature Protocols (Chamma et al., sous presse). Nous espérons que cette technique pourra être adoptée par un grand nombre de neuroscientifiques, pour la détection et caractérisation de structures sub-cellulaires neuronales.
CHAMMA I, LETELLIER M, Butler, Tessier B, Lim KH, Gauthereau I, Choquet D, Sibarita JB, Park S, Sainlos M*, THOUMINE O* (*Co-last authors).
Mapping the dynamics and nanoscale organization of synaptic adhesion proteins using monomeric streptavidin.
Nat Comm 2016, Mar 16;7:10773. doi: 10.1038/ncomms10773.
Subventions ERC 2016 pour 4 neurobiologistes français

Quatre neurobiologistes français lauréats des ERC Consolidator Grants :
Karim BENCHENANE, Equipe Memory, Oscillations & Brain States, Brain Plasticity Unit, UMR 8249 CNRS, ESPCI-ParisTech, Paris, pour son projet MNEMOSYNE
« Brain computer interface to study and manipulate memories of aversive experience during sleep »,
Paolo GIACOBINI, Equipe Development & Plasticity of the Neuroendocrine Brain, U1172 INSERM, Lille pour son projet REPRODAM
« Extra-gonadal roles of Anti-Müllerian Hormone in the aetiology of polycystic ovary syndrome: the domino effect to reproductive neuroendocrine dysfunctions »
Fekrije SELIMI, Centre Interdisciplinaire de Recherche en Biologie (CIRB), Collège de France, CNRS UMR 7241 – INSERM U1050 pour son projet SynID
« Activity-dependent modulation of synapse identity »
German SUMBRE, Equipe Développement et Plasticité du Cerveau, IBENS-Ecole Normale Supérieure, CNRS UMR 8197 – INSERM U1024, Paris pour son projet Spontaneous ZeBrain
« Whole-brain dynamics underlying self-generated behaviour »
Des molécules qui ont le rythme

Des corpuscules du noyau de la cellule font rythmer l’expression des gènes sur 24 heures
Pour s’adapter à l’alternance quotidienne de jour et de nuit, tous les organismes ont développé une rythmicité de leurs fonctions sur 24 heures. Au niveau cellulaire, de nombreux gènes suivent une telle rythmicité dont les mécanismes restent méconnus. L’équipe d’Anne-Marie François-Bellan au Centre de recherche en neurobiologie- neurophysiologie de Marseille révèle l’implication dans cette expression rythmique de corpuscules nucléaires dont le nombre varie au cours de 24 heures et le ciblage thérapeutique pourrait permettre de contrôler les pathologies associées à des dysfonctionnements rythmiques. Cette étude est publiée dans la revue eLife.
L’adaptation aux contraintes d’un environnement en évolution permanente impose aux êtres vivants des fluctuations rythmiques de leurs paramètres biologiques. Ces fluctuations concernent une multitude de processus, depuis le métabolisme cellulaire jusqu’aux activités comportementales et physiologiques y compris la température corporelle, la pression sanguine et les taux d’hormones. Les recherches en chronobiologie ont permis de montrer à quel point cette rythmicité, et en particulier sa composante dite « circadienne » pour exprimer le fait qu’elle se manifeste sur une base proche de 24h, est une composante essentielle de cette adaptation des êtres vivants. C’est vraisemblablement parce qu’ils jouent un rôle primordial en tant que mécanismes adaptatifs indispensables à la survie que le dérèglement des rythmes circadiens est associé à de nombreuses pathologies dont les plus étudiées sont les pathologies hormonales et métaboliques, cardiovasculaires, neuropsychiatriques et les cancers slimming tablets.
La rythmicité de bon nombre de fonctions biologiques repose en partie sur la rythmicité d’expression d’ARNm au sein de la cellule. On sait aujourd’hui, contrairement aux idées initiales, que la rythmicité de la majorité des ARNm ne repose pas sur une transcription rythmique. Il est en effet récemment apparu que si jusqu’à 20% des gènes exprimés dans un organe présentent un profil rythmique, seulement 20% des ARNm rythmiques sont contrôlés au niveau transcriptionnel. Un des enjeux actuels en chronobiologie est la recherche de ces mécanismes largement méconnus qui s’exercent après la transcription et sont impliqués dans la régulation des rythmes circadiens.
L’équipe d’Anne-Marie François-Bellan a caractérisé un de ces mécanismes post-transcriptionnels qui permet l’expression rythmique d’ARNm dans des cellules de l’hypophyse. Ce mécanisme implique un long ARN non-codant, Neat1 (Nuclear-Enriched Abundant Transcript 1) dont l’expression rythmique a pu être mise en évidence non seulement dans les cellules hypophysaires mais également dans de nombreux autres oscillateurs circadiens ainsi que dans l’horloge hypothalamique circadienne. Ce long ARN non-codant sert de matrice d’assemblage pour des protéines de liaison aux ARN, l’ensemble formant des corpuscules nucléaires appelés paraspeckles. Les chercheurs ont montré que tous les composants des paraspeckles ainsi que le nombre des paraspeckles, présentent une rythmicité circadienne d’expression et d’association à l’intérieur des cellules hypophysaires.
Bien que leur fonction soit largement méconnue, on sait que ces paraspeckles peuvent entrainer une rétention nucléaire d’ARNm lorsque ceux-ci présentent dans leur région 3’UTR des séquences répétées et inversées de type Alu (IRAlu), ce qui empêche leur export cytoplasmique et permet le contrôle de leur niveau d’expression. Les chercheurs ont alors émis l’hypothèse selon laquelle la rythmicité du nombre de ces corps nucléaires pourrait permettre la rythmicité circadienne des ARNm qu’ils retiennent dans le noyau. De fait, ils ont montré que l’insertion d’une séquence IRAlu dans la région 3’UTR du gène rapporteur egfp, induit une rétention nucléaire rythmique de l’ARNm egfp. Cette rétention est abolie après destruction des paraspeckles par des siRNA ou des oligonucléotides antisens de Neat1. Par vidéo microscopie en temps réel, ils ont montré que cette séquence IRAlu en 3’UTR de l’egfp entraîne une expression cytoplasmique rythmique de la protéine EGFP. Grâce à une technique de précipitation spécifique de l’ARN Neat1, ils ont isolé et, après séquençage haut débit, identifié l’ensemble des ARNm associés à Neat1. A partir d’exemples d’ARNm sélectionnés dans cette liste, ils ont montré que les ARNm associés à Neat1 présentent une rétention nucléaire rythmique abolie après destruction des paraspeckles.
Ces résultats montrent que les paraspeckles, grâce à leur expression circadienne, peuvent contrôler la rythmicité circadienne d’expression des ARNm qui leur sont associés et permettent de proposer un nouveau mécanisme post-transcriptionnel original impliqué dans le fonctionnement du système circadien.
Le ciblage thérapeutique des paraspeckles pourrait être à la base de nouvelles stratégies permettant de contrôler les rythmes circadiens, avec l’objectif d’améliorer les situations, en pathologique humaine, qui sont associées à un dysfonctionnement de la rythmicité des fonctions, en particulier des fonctions hormonales. Outre le décryptage d’un mécanisme post-transcriptionnel impliqué dans la régulation circadienne de l’expression de gènes, une problématique ancrée dans le domaine de la chronobiologie, cette étude, dans le domaine de l’endocrinologie fondamentale et/ou clinique, permet d’attribuer un rôle, dans la physiologie et la pathologie de l’hypophyse, à ce long ARN non-codant, Neat1, dont les fonctions demeurent énigmatiques.
Ce travail a bénéficié d’un prix de recherche Pfizer-Société Française d’Endocrinologie
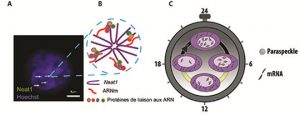
Figure : Structure des paraspeckles et implication fonctionnelle dans l’expression rythmique d’ARNm. A : Visualisation des paraspeckles identifiés par leur constituant principal, le long ARN non-codant, Neat1, à l’intérieur du noyau des cellules coloré en bleu par le colorant de Hoechst. B : Organisation schématique des différents constituants des paraspeckles. C : La rythmicité du nombre de paraspeckles à l’intérieur du noyau permet le contrôle de l’expression des ARNm associés.
© Anne-Marie François-Bellan
En savoir plus
Circadian RNA expression elicited by 3′-UTR IRAlu-paraspeckle associated elements.
Torres M, Becquet D, Blanchard MP, Guillen S, Boyer B, Moreno M, Franc JL, François-Bellan AM.
Elife. 2016 Jul 21;5. pii: e14837. doi: 10.7554/eLife.14837.
Contact chercheur
Anne-Marie François-Bellan
Centre de recherche en neurobiologie – neurophysiologie de Marseille (CRN2M)
CNRS UMR 7286. Université Aix-Marseille
Faculté de Médecine Secteur Nord
51 Boulevard Pierre Dramard
13344 Marseille cedex 15
Tel: 04 91 69 89 07
Les mitochondries sont essentielles à la mémoire

De nombreuses études ont montré que la prise de cannabis peut entraîner des pertes de mémoire à court et à long terme. Ces effets sur la mémoire seraient liés à la présence de récepteurs spécifiques sur plusieurs types cellulaires cérébraux (neurones mais aussi cellules gliales). Des chercheurs de l’Inserm sous la direction de Giovanni Marsicano (NeuroCentre Magendie, U1215) montrent que ces effets sur la mémoire sont liés à la présence de ces mêmes récepteurs sur les mitochondries, la centrale énergétique des cellules. C’est la première fois que l’implication directe des mitochondries dans les fonctions supérieures du cerveau, comme l’apprentissage et la mémoire, est montrée.
Ces travaux sont publiés dans la revue Nature.
Les mitochondries sont les centrales énergétiques des cellules animales. Elles sont présentes à l’intérieur des cellules pour produire l’énergie (sous forme d’ATP) nécessaire à tous les processus biochimiques. Pour ce faire, elles utilisent l’oxygène pour transformer les nutriments en ATP. Ces fonctions sont évidemment nécessaires à la survie de l’ensemble des cellules du corps, mais dans le cerveau l’impact des mitochondries va au de-là de la simple survie cellulaire. Si le cerveau ne représente que 2% du poids du corps, il consomme en effet, jusqu’à 25% de son énergie. Par conséquent, l’équilibre énergétique du cerveau est quelque chose de très important pour ses fonctions et, donc très régulé. On sait parfaitement que des altérations chroniques des fonctions mitochondriales (par ex. dans les maladies mitochondriales) produisent d’importants symptômes neurologiques et neuropsychiatriques.
Cependant, l’implication fonctionnelle directe des mitochondries dans les fonctions supérieures du cerveau, comme l’apprentissage et la mémoire, était jusqu’à présent inconnue. En d’autres termes, nous servons-nous des mitochondries de notre cerveau quand nous apprenons ou quand nous nous souvenons de quelque chose ?
Cette étude, qui s’appuie sur la découverte du fait que le récepteur cannabinoïde CB1 est aussi présent sur les mitochondries du cerveau (appelées mtCB1) révèle que c’est bien le cas. À l’aide d’outils innovants, les chercheurs de l’Inserm ont montré que le composant actif du cannabis, le THC (delta9-tétrahydrocannabinol), provoque de l’amnésie chez les souris en activant les mtCB1 dans l’hippocampe.
« La diminution de mémoire induite par le cannabis chez la souris exige l’activation de ces récepteurs mtCB1 hippocampiques » explique Giovanni Marsicano. A l’inverse, « leur suppression génétique empêche cet effet induit par la molécule active du cannabis. Nous pensons donc que les mitochondries développent notre mémoire en apportant de l’énergie aux cellules du cerveau ».
Cette étude est importante non seulement parce qu’elle présente un nouveau mécanisme qui sous-tend les effets du cannabis sur la mémoire, mais aussi parce qu’elle révèle que l’activité mitochondriale fait partie intégrante des fonctions du cerveau.
Communiqué – Salle de Presse Inserm
Les mitochondries sont essentielles à la mémoire
Source :
A cannabinoid link between mitochondria and memory.
Hebert-Chatelain E, Desprez T, Serrat R, Bellocchio L, Soria-Gomez E, Busquets-Garcia A, Pagano Zottola AC, Delamarre A, Cannich A, Vincent P, Varilh M, Robin LM, Terral G, García-Fernández MD, Colavita M, Mazier W, Drago F, Puente N, Reguero L, Elezgarai I, Dupuy JW, Cota D, Lopez-Rodriguez ML, Barreda-Gómez G, Massa F, Grandes P, Bénard G, Marsicano G.
Nature. 2016 Nov 9;539(7630):555-559
Contact chercheur :
Giovanni Marsicano
Unité Inserm 1215 « Neurocentre Magendie » (Inserm/Université de Bordeaux)
Group « Endocannabinoids and Neuroadaptation »
Tel. 05 57 57 37 56
Contact presse : presse@inserm.fr
Illustration : © Charlie Padgett