Uncategorized
Les bases neuronales de la phototaxis chez le poisson zèbre.
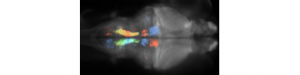
L’équipe de Georges Debrégeas au sein du Laboratoire Jean Perrin de l’Université Pierre et Marie Curie à Paris a récemment découvert les bases neuronales de la phototaxis chez le poisson zèbre. A l’état larvaire, le poisson zèbre a la capacité de naviguer vers les zones les plus lumineuses de son environnement, un comportement qu’on observe chez de nombreux organismes.
L’équipe de chercheurs a montré que l’activité d’un ensemble de neurones localisé dans le cerveau postérieur (hindbrain) du poisson zèbre appelé Hindbrain Oscillator (HBO) permet d’expliquer la phototaxis chez cet animal. En combinant des méthodes d’imagerie par nappe laser permettant d’enregistrer l’activité de l’ensemble des neurones du poisson zèbre ainsi que des techniques optogénétiques, les chercheurs ont découvert que ce HBO est une population neuronale auto-oscillante, qui contrôle la direction du regard de l’animal ainsi que l’orientation de ses mouvements de nage. L’utilisation d’un microscope à nappe laser deux photons leur a ensuite permis de découvrir que cette population neuonale est sensible à des inputs visuels de telle sorte que sa réponse dépende du contexte moteur i.e. la position des yeux. Cette réponse particulière à des stimulations visuelles biaise la navigation du poisson zèbre en direction des zones les plus lumineuses lui permettant ainsi de faire de la phototaxis
Référence
Wolf S, Dubreuil AM, Bertoni T, Böhm UL, Bormuth V, Candelier R, Karpenko S, Hildebrand DGC, Bianco IH, Monasson R, Debrégeas G. Sensorimotor computation underlying phototaxis in zebrafish. Nat Commun. 2017 Sep 21;8(1):651. doi: 10.1038/s41467-017-00310-3.
https://www-ncbi-nlm-nih-gov.gate2.inist.fr/pmc/articles/PMC5608914/
Contact
Georges Debregeas
Laboratoire Jean Perrin, UMR UPMC-CNRS 8237
4 place Jussieu, 75005 PARIS
georges.debregeas@upmc.fr
Concours “Dance your Ph.D.”

La Société des Neurosciences encourage et soutient la participation de ses membres au concours “Dance your Ph.D.”, sponsorisé par la revue Science et l’AAAS, une initiative d’information sur la recherche scientifique à visée du grand public. Il s’agit d’expliquer et d’interpréter son sujet de thèse de façon ludique, dans une danse qui pourra être primée et diffusée sur internet.
Dans le cadre de l’édition 2017 de ce concours, Romain Durand-de Cuttoli, étudiant en thèse au sein de l’équipe “Neurophysiologie et comportements” dirigée par P. Faure et Alexandre Mourot (Unité Neurosciences Paris Seine) propose une vidéo : “Purple Brain: Optically disrupting the rewarding properties of nicotine”.
Vous pouvez regarder la vidéo en suivant ce lien: https://www.youtube.com/watch?v=47Men_s78_E&sns=fb
Et “liker” afin d’augmenter les chances du candidat !
Plasticité et mobilité, les clefs de la mémoire !
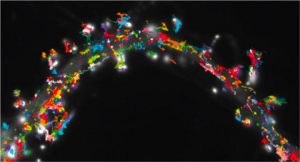
Communiqué de presse du CNRS: http://www2.cnrs.fr/presse/communique/5183.htm
Dans un effort commun, les équipes de Daniel Choquet et de Yann Humeau de l’Institut de Neuroscience Interdisciplinaire (CNRS/Université de Bordeaux) à Bordeaux et du Bordeaux Imaging Center (CNRS/Université de Bordeaux/Inserm) ont découvert récemment un mécanisme pour le stockage de l’information dans les synapses et un moyen pour contrôler ce processus de stockage.
Il y a quelques années, l’équipe de chercheurs bordelais avait découvert que les récepteurs de neurotransmetteurs n’étaient pas immobiles comme on le pensait, mais au contraire en agitation permanente. Ils avaient alors suggéré que le contrôle de cette agitation par l’activité neuronale pouvait être capable de moduler l’efficacité de la transmission synaptique en contrôlant le nombre de récepteurs présents à un instant donné dans une synapse.
Dans ces nouveaux travaux, les deux équipes sont allées plus loin dans la compréhension des mécanismes fondamentaux de stockage de l’information dans le cerveau.
Les chercheurs ont combiné des techniques de chimie, d’électrophysiologie et d’imagerie à haute résolution pour mettre au point une méthode inédite d’immobilisation des récepteurs au niveau des synapses. Grâce à cette méthode, les mouvements des récepteurs sont stoppés, ce qui permet d’étudier l’impact de leur immobilisation sur l’activité cérébrale et les capacités d’apprentissage.
Ils ont ainsi démontré que le mouvement des récepteurs est indispensable aux processus de plasticité synaptique en réponse à une activité neuronale intense. Ils ont ensuite exploré le rôle direct de la plasticité des synapses dans l’apprentissage. En apprenant à des souris à reconnaitre un environnement particulier, ils ont pu mettre en évidence que le gel du mouvement des récepteurs permet de bloquer l’acquisition de cette forme de mémoire, démontrant ainsi l’implication de la plasticité synaptique dans ce processus.
Référence:
Hippocampal LTP and contextual learning require surface diffusion of AMPA receptors. Penn A.C., Zhang C.L., Georges F., Royer L., Breillat C., Hosy E., Petersen J.D., Humeau Y. and Choquet D. Nature, le 13 septembre 2017. DOI : 10.1038/nature23658
Effet de l’activité synaptique sur l’agrégation de la protéine tau: une observation clé pour la compréhension des Tauopathies
La diminution du métabolisme cérébral et les altérations de l’excitabilité synaptique sont les premiers événements associés au développement de la démence, incluant la maladie d’Alzheimer (MA) et la démence frontotemporale (DFT). Pour contrecarrer l’hypométabolisme et le dysfonctionnement des synapses, la stimulation synaptique représente une approche thérapeutique importante contre la MA. En effet, de nombreuses études ont montré que la stimulation cérébrale profonde exerce des effets bénéfiques chez les patients atteints de la MA.
Parmi les formes pathologiques de la protéine tau associées à la MA et à la DFT, les formes hyperphosphorylées et agrégées sont considérées comme les plus toxiques. Le docteur Davide Tampellini et ses collègues chercheurs au Kremlin-Bicêtre (Institut Professeur Baulieu/U 1195 Inserm), en collaboration avec une équipe nord américaine, italienne, française et espagnole, a mis en évidence les effets inverses de la stimulation cérébrale d’une part et de l’inhibition synaptique chronique d’autre part, dans des modèles in vivo et in vitro de ces tauopathies. La stimulation cérébrale profonde du cortex entorhinal de souris transgéniques de la MA (3xTg) a conduit à la réduction des formes pathologiques de tau et la protection des synapses, tandis que l’inhibition de l’activité synaptique par une déafférentation unilatérale du cortex somatosensoriel de souris transgéniques de la DFT a entraîné une accumulation massive d’oligomères de tau dans les lysosomes élargis, avec une détérioration accrue des synapses.
La stimulation synaptique a exercé une protection neuronale par un mécanisme de dégradation de la protéine tau pathologique impliquant le système autophagosome-lysosome. Notre étude a démontré que les autophagosomes étaient responsables de la livraison d’oligomères de tau aux lysosomes. En fait, le blocage de l’autophagie a réduit le nombre d’oligomères dans les somas et les lysosomes, et a accru leur accumulation dans les neurites. De plus, l’activation synaptique a augmenté la maturation de la cathepsine D et l’activité lysosomale, renforçant ainsi la dégradation de la protéine tau pathologique.
Ces données originales apportent la preuve du rôle protecteur de la stimulation synaptique contre les effets des formes pathologiques de tau dans la MA et la DFT, ainsi qu’un rationnel pour l’utilisation de thérapies telle que la stimulation cérébrale profonde pour maintenir l’activité cérébrale/synaptique.
La diminution du métabolisme cérébral et les altérations de l’excitabilité synaptique sont les premiers événements associés au développement de la démence, incluant la maladie d’Alzheimer (MA) et la démence frontotemporale (DFT). Pour contrecarrer l’hypométabolisme et le dysfonctionnement des synapses, la stimulation synaptique représente une approche thérapeutique importante contre la MA. En effet, de nombreuses études ont montré que la stimulation cérébrale profonde exerce des effets bénéfiques chez les patients atteints de la MA.
Parmi les formes pathologiques de la protéine tau associées à la MA et à la DFT, les formes hyperphosphorylées et agrégées sont considérées comme les plus toxiques. Le docteur Davide Tampellini et ses collègues chercheurs au Kremlin-Bicêtre (Institut Professeur Baulieu/U 1195 Inserm), en collaboration avec une équipe nord américaine, italienne, française et espagnole, a mis en évidence les effets inverses de la stimulation cérébrale d’une part et de l’inhibition synaptique chronique d’autre part, dans des modèles in vivo et in vitro de ces tauopathies. La stimulation cérébrale profonde du cortex entorhinal de souris transgéniques de la MA (3xTg) a conduit à la réduction des formes pathologiques de tau et la protection des synapses, tandis que l’inhibition de l’activité synaptique par une déafférentation unilatérale du cortex somatosensoriel de souris transgéniques de la DFT a entraîné une accumulation massive d’oligomères de tau dans les lysosomes élargis, avec une détérioration accrue des synapses.
La stimulation synaptique a exercé une protection neuronale par un mécanisme de dégradation de la protéine tau pathologique impliquant le système autophagosome-lysosome. Notre étude a démontré que les autophagosomes étaient responsables de la livraison d’oligomères de tau aux lysosomes. En fait, le blocage de l’autophagie a réduit le nombre d’oligomères dans les somas et les lysosomes, et a accru leur accumulation dans les neurites. De plus, l’activation synaptique a augmenté la maturation de la cathepsine D et l’activité lysosomale, renforçant ainsi la dégradation de la protéine tau pathologique.
Ces données originales apportent la preuve du rôle protecteur de la stimulation synaptique contre les effets des formes pathologiques de tau dans la MA et la DFT, ainsi qu’un rationnel pour l’utilisation de thérapies telle que la stimulation cérébrale profonde pour maintenir l’activité cérébrale/synaptique.
Référence :
Akwa Y, Gondard E, Mann A, Capetillo-Zarate E, Alberdi E, Matute C, Marty S, Vaccari T, Lozano AM, Baulieu EE, Tampellini D. Synaptic activity protects against AD and FTD-like pathology via autophagic-lysosomal degradation. Mol Psychiatry. 2017 Jul 11. doi: 10.1038/mp.2017.142
Contact :
Davide Tampellini, Ph.D.
Institut Professeur Baulieu, Bât. Gregory Pincus, 2eme étage
U 1195 Inserm – Université Paris Sud – Université Paris-Saclay
80, rue du General Leclerc
94276 Le Kremlin-Bicetre Cedex
France
Rôle de l’insuline dans le cerveau : un rôle inédit de la protéine Tau !
La protéine Tau est une des protéines majeures qui s’agrègent pour conduire à la mort neuronale dans de nombreuses maladies neurodégénératives, dont la maladie d’Alzheimer. Il s’agit d’une protéine associée aux microtubules mais qui possède bien d’autres fonctions encore méconnues. David Blum et Luc Buée de l’équipe « Alzheimer & Tauopathies », UMR-S1172 (Université de Lille CHU de Lille Inserm) viennent de démontrer qu’une fonction physiologique de la protéine Tau est de réguler les effets de l’insuline dans le cerveau. L’insuline, une hormone sécrétée par les cellules du pancréas, exerce, au niveau périphérique, une action cruciale dans le contrôle de l’homéostasie glucidique. Elle a également des actions multiples dans le cerveau en favorisant non seulement la plasticité et la mémoire mais modulant également la prise alimentaire et l’homéostasie périphérique. Les chercheurs ont démontré que les actions de l’insuline dans le cerveau étaient réduites chez des animaux ne possédant pas la protéine Tau. Ainsi, les souris déficientes en Tau présentent une réponse réduite à l’insuline au niveau de l’hippocampe, une structure du cerveau impliquée dans la mémoire. L’absence de protéine Tau provoque également des troubles du métabolisme chez les souris comme un gain anormal de poids et une intolérance au glucose, des manifestations généralement associées à l’obésité ou au diabète. Ces effets métaboliques seraient la conséquence d’une diminution des effets de l’insuline dans le cerveau, notamment sa capacité à réduire la prise alimentaire. Ce rôle de la protéine Tau est étayé par des données génétiques chez l’Homme. Cette étude fournit la première preuve d’un rôle de la protéine Tau dans les effets de l’insuline au niveau du cerveau et apporte de nouvelles pistes dans la compréhension des maladies neurodégénératives et des troubles métaboliques associés à ces pathologies.
Ces travaux ont fait l’objet d’un soutien de France Alzheimer/Fondation de France et du projet Fédératif Hospitalo-Universitaire (FHU) VasCog financé par le CHU de Lille et l’Université de Lille. L’équipe « Alzheimer & Tauopathies » appartient au LabEx DISTALZ (development of Innovative Strategies for a Transdisciplinary Approach to Alzheimer’s Disease) et au LiCEND (Lille Centre of Excellence in Neurodegenerative Disorders). Ces travaux impliquent différents laboratoires français et européens : U1011-EGID (Lille), U1016 CNRS UMR8104 (Institut Cochin, Paris), U1167-RID AGE (Lille), Laboratory of Biological Psychology, KU Leuven, Belgium, Department of Experimental Neurodegeneration, University Medical Center Goettingen, Germany
Source
Marciniak E, Leboucher A, Caron E, Ahmed T, Tailleux A, Dumont J, Issad T, Gerhardt E, Pagesy P, Vileno M, Bournonville C, Hamdane M, Bantubungi K, Lancel S, Demeyer D, Eddarkaoui S, Vallez A, Vieau D, Humez S, Faivre E, Grenier-Boley B, Outeiro TH, Staels B, Amouyel P, Balschun D, Buee L & Blum D. Tau deletion promotes brain insulin resistance (2017) The Journal of Experimental Medicine doi: 10.1084/jem.20161731.
Lien
http://jem.rupress.org/content/early/2017/06/23/jem.20161731.long
Contact chercheur
David Blum, Directeur de Recherche
UMR-S1172 “Centre de recherche Jean Pierre Aubert
“Alzheimer & Tauopathies” – LabEx DISTALZ
Faculté de Médecine-Pôle Recherche
59045 Lille France
david.blum@inserm.fr
Tel: 03 20 29 88 50
Concours Photos 2017
Sébastien Brot
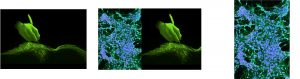
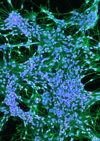 Neurones cultivés in vitro, différenciés à partir de cellules IPS humaines.
Neurones cultivés in vitro, différenciés à partir de cellules IPS humaines.
En vert, la protéine GFP exprimée de façon constitutive, en rouge le marqueur de neurones matures NeuN Foxa2 et en bleu, le marquage DAPI.
Université de Poitiers, Laboratoire de Neurosciences Expérimentales et Clinique (INSERM U1084)
Delphine Prieur
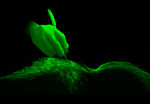 The brain’s diary
The brain’s diary
Axons of electroporated retinal ganglion cells in the optic tract and invading their brain target (dLGN) (fluorescence microscopy), and photography of a PhD student hand.
Institut du Fer à Moulin, Paris
Une avancée majeure pour la compréhension des ataxies cérébelleuses
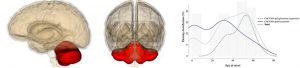
Des chercheurs de l’Institut du Cerveau et de la Moëlle Epinière (ICM) à l’Hôpital de la Pitié-Salpetrière à Paris viennent de publier une large étude de génétique épidémiologique portant sur 412 patients atteints d’ataxie cérébelleuse autosomique dominante.
L’hétérogénéité génétique de ces maladies, qui touchent le cervelet et affecte la coordination et l’équilibre et peuvent être causées par des mutations dans plus de 40 gènes, rend leur diagnostic génétique compliqué. Le plus fréquemment, la mutation incriminée est une expansion d’une répétition d’une courte séquence de nucléotides, telle qu’un triplet « CAG ». Dans de plus rares cas, on est en présence de mutations plus « conventionnelles ». Si l’épidémiologie des formes dites à expansion a été bien étudiée, ce n’est pas le cas de ces dernières.
Les chercheurs ont conçu un panel permettant de séquencer en une fois l’ensemble des 34 gènes connus pour présenter ce type de mutations dans les ataxies cérébelleuses, et l’ont utilisé chez 412 patients qui ne présentaient pas d’expansion de répétition. Cela leur a permis d’identifier une mutation responsable chez près de 15% des patients auparavant non diagnostiqués. Les gènes codant pour des canaux ioniques étaient les plus fréquemment mutés, ce qui confirme leur importance majeure dans le fonctionnement du cervelet.
Ils ont aussi comparé les présentations cliniques de l’ataxie cérébelleuse entre des patients porteurs d’une expansion et des patients présentant une mutation conventionnelle. Ces derniers commencent souvent la maladie plus tôt, mais montrent une progression plus lente et un phénotype plus pur, avec moins d’autres signes accompagnateurs.
Cette étude, en plus d’apporter un diagnostic précis à une proportion non négligeable de patients, permet donc de mieux caractériser les aspects génétiques et cliniques des ataxies cérébelleuses autosomiques dominantes, ce qui améliorera la prise en charge et le conseil génétique pour les patients.
Référence de l’article:
A panel study on patients with dominant cerebellar ataxia highlights the frequency of channelopathies.
Coutelier M, Coarelli G, Monin ML, Konop J, Davoine CS, Tesson C, Valter R, Anheim M, Behin A, Castelnovo G, Charles P, David A, Ewenczyk C, Fradin M, Goizet C, Hannequin D, Labauge P, Riant F, Sarda P, Sznajer Y, Tison F, Ullmann U, Van Maldergem L, Mochel F, Brice A, Stevanin G, Durr A; SPATAX network. Brain. 2017 Jun 1;140(6):1579-1594. doi: 10.1093/brain/awx081.
Lien vers l’article: https://academic.oup.com/brain/article-lookup/doi/10.1093/brain/awx081
Contact:
Dr Alexandra Durr
Reference centre for Rare diseases-Neurogenetics
ICM (Institut du Cerveau et de la Moelle épinière)
Salpêtrière Hospital – Université Pierre et Marie Curie
47 boulevard de l’Hôpital
75651 Paris CEDEX 13
alexandra.durr@icm-institute.org
Marches pour les Sciences

Le 22 avril, auront lieu dans le monde entier, des “Marches pour les sciences”.
La Société des Neurosciences, comme la FENS et de nombreuses sociétés scientifiques internationales, s’associe à cette action qui a pour objectif de mettre en avant l’importance pour le bien commun et la civilisation de la démarche scientifique, respectant les faits et l’honnêteté intellectuelle, ouverte à tous dans le monde entier.
Pour plus d’information sur les actions en France :
un anxiolytique naturellement efficace !

Des chercheurs de l’Institut des maladies neurodégénératives de Bordeaux (IMN-UMR-CNRS 5293 / Université de Bordeaux) viennent de découvrir que les réactions anxieuses occasionnées par des facteurs de stress pourraient être le reflet des changements synaptiques qui s’opèrent dans une petite région du cerveau : Le noyau du lit de la strie terminale (BNST). A travers des expériences conduites chez des rats exposés à des situations anxiogènes, les chercheurs ont disséqué un circuit neuronal qui, lorsqu’il est activé, réduit les niveaux d’anxiété de l’animal pendant plusieurs jours. Ces résultats, issus d’une collaboration entre deux laboratoires bordelais (IMN-UMR-CNRS 5293 et INCIA-UMR-CNRS 5287) et un laboratoire suisse (FMI, Basel, Switzerland) sont publiés dans Nature Communications, le 20 Février 2017.
L’anxiété est une émotion physiologique qui déclenche un état d’alerte en réponse à une menace réelle ou supposée et constitue ainsi un mécanisme de survie. Le noyau du lit de la stria terminalis (BNST) appartient à un réseau neuronal de régions limbiques interconnectées et exerce un rôle central dans l’expression de l’anxiété chez de nombreuses espèces animales, et notamment chez l’Homme. Les auteurs de l’étude ont utilisé des approches virales pour tracer les voies neuronales dans trois régions cérébrales impliquées dans les comportements associés à l’état d’anxiété. Ils ont enregistré et manipulé, in vivo, l’activité électrique des neurones. Ils ont ainsi mis en évidence qu’une population de neurones du BNST (centre cérébral de la motivation et de l’anxiété), intégrait et filtrait des informations en provenance du subiculum ventral (centre cérébral de la mémoire des émotions) et du cortex infralimbique (centre cérébral de la mémoire et des habitudes) pour augmenter de façon persistante leur activité. Les conséquences de ce changement d’état des neurones du BNST sont, en particulier des changements d’état anxieux de l’animal.
Les chercheurs ont ainsi pu déterminer que la mise en place d’une plasticité de type potentialisation à long terme au niveau des synapses « subiculum ventral/BNST » provoque un effet activateur et persistant (plusieurs jours) sur les neurones du BNST ayant pour conséquence de jouer le rôle d’un anxiolytique.
Ce travail, en précisant les circuits neuronaux et mécanismes de plasticité synaptique qui réduisent les niveaux d’anxiété de l’animal de manière persistante, ouvre de nouvelles perspectives pour comprendre comment un changement de l’état synaptique des neurones du BNST pourrait modifier la perception de stimuli sensoriels en condition pathologique (addiction, trouble de l’anxiété). Ces travaux ont été financés notamment par l’Agence nationale pour la recherche (ANR), le CNRS et l’université de Bordeaux.
Référence:
NMDA-receptor-dependent plasticity in the bed nucleus of the stria terminalis triggers long-term anxiolysis.Glangetas C, Massi L, Fois GR, Jalabert M, Girard D, Diana M, Yonehara K, Roska B, Xu C, Lüthi A, Caille S, Georges F. Nat Commun. 2017 Feb 20;8:14456.
Contact auteur : Dr François GEORGES, CNRS/Université de Bordeaux : francois.georges@u-bordeaux.fr / Tel : +33 5 33 51 48 13
Hightlights NeuroFrance 2017

NeuroFrance 2017, un programme plus dense, plus riche :
7 conférenciers pléniers de renommée internationale, 42 symposiums, des symposiums spécialisés, des sessions “Réussir avec une thèse en neurosciences”, lectures de CV et courts entretiens, près de 600 posters
Une exposition commerciale de plus de 45 stands
NeuroNight : pour une soirée mémorable en bord de Garonne !
Ne ratez pas l’occasion de participer et de découvrir Bordeaux, numéro 1 des villes à visiter en 2017 selon le Lonely Planet !
Inscrivez-vous avant le 5 avril pour bénéficier des tarifs préférentiels !