Divers
Paris capitale des neurosciences en 2022 !

La Société des Neurosciences se félicite du choix de Paris pour accueillir le FENS Forum 2022 !
Il faut être trois pour danser le tango : la synapse tripartite révélée par la microscopie superresolutive

Les astrocytes sont les cellules gliales les plus nombreuses dans le cerveau. Elles utilisent les signaux calciques pour réguler leur activité biochimique et communiquer avec les autres cellules du cerveau. Alors que chaque astrocyte est en principe bien placé pour influencer avec une grande dextérité les milliers de connexions synaptiques qui se trouvent dans leurs domaines anatomiques respectifs, les signaux calciques astrocytaires ont longtemps été considérés comme trop lents et diffus pour servir de médiateurs à tout type d’actions rapides et spécifiques. Cependant, cette idée résulte d’études contraintes par une microscopie à faible résolution, qui ne peut accéder aux signalisations calciques que dans les compartiments cellulaires les plus gros tels que le corps cellulaire et les principaux prolongements émergent de celui-ci. Des travaux plus récents ont cependant montré que des signaux calciques rapides et localisés pouvaient être générés dans les prolongements astrocytaires extrêmement fins qui interagissent directement avec les synapses, rappelant ainsi les signaux utilisés par les neurones pour opérer une communication point-à-point à grande vitesse. Cependant, la base morphologique de ces signaux astrocytaires rapides et localisés n’était pas connue, en raison des difficultés à résoudre la morphologie complexe des astrocytes (et des synapses), tout en enregistrant leur activité calcique dans le tissu cérébral vivant. Pour surmonter ce problème, nous nous sommes tournés vers la microscopie 3D-STED, qui offre une résolution spatiale beaucoup plus élevée que la microscopie optique classique et permet de révéler la morphologie des astrocytes et des neurones de manière très détaillée. En combinant ce type de microscopie avec l’imagerie confocale calcique permettant de mesurer l’activité calcique, et des expériences de FRAP pour évaluer les propriétés biophysiques, nous avons pu élucider les bases anatomiques des signaux calciques dans les astrocytes. Nous avons observé que les prolongements astrocytaires forment un réseau réticulaire de nœuds et de branches qui s’organisent autour de structures en forme d’anneau. Les nœuds présentent des signaux calciques spontanés, localisés la plupart du temps, mais qui peuvent également se propager aux nœuds voisins via des structures en branches. Les expériences de FRAP ont montré que cette organisation permet une signalisation compartimentée, mais aussi la propagation du signal à travers plusieurs nœuds. La superposition des données calciques avec la morphologie fine des structures astrocytaires a révélé que la majorité des signaux calciques sont associés à des synapses individuelles, ce qui suggère que les astrocytes sont capables d’engager une communication avec des synapses spécifiques. Notre étude apporte donc un nouvel éclairage sur l’organisation à l’échelle nanométrique des astrocytes dans le tissu cérébral vivant (tranches organotypiques et aiguës et in vivo), en révélant une organisation en « nœuds » pouvant réguler la communication neuronale à l’échelle de « synapses tripartites » individuelles.
It takes three to tango: the tripartite synapse revealed by super-resolution microscopy
Astrocytes, which are the most numerous glial cells in the brain, use Ca2+ signals to regulate their biochemical activity and communication with other brain cells. While single astrocytes are in principle well positioned to influence thousands of neuronal synapses that lie within their anatomical domain with great dexterity, astrocytic Ca2+ signals have long been thought to be too sluggish and sprawling for mediating any type of fast and specific actions. However, this view has come from low-resolution studies that have looked at the soma and major branches of the astrocytes. More recent work on the tiny but relevant astrocytic processes that actually contact synapses suggests that the situation may be similar to neurons, where fast and local synaptic Ca2+ signals mediate high-speed point-to-point communication. However, the anatomical basis of such specific signaling by astrocytes has remained unclear, owing to difficulties in resolving the complex morphology of astrocytes (and synapses), while also recording their Ca2+ activity in live brain tissue.
To overcome this problem, we turned to 3D-STED microscopy, which offers a much higher spatial resolution than regular light microscopy and can reveal the morphology of astrocytes and neurons in great detail. By combining it with confocal Ca2+ imaging to monitor Ca2+ activity, and FRAP experiments to assess biophysical properties, we could elucidate the anatomical basis of Ca2+ signals in astrocytes. We observed that astrocytic processes form a reticular meshwork of nodes and shafts that formed ring-like structures. The nodes exhibited spontaneous Ca2+ signals that stayed local most of the time, but could also spread to neighboring nodes via the shafts. FRAP experiments established that the astrocytic node/shaft structure generally supports compartmentalized signaling, yet also permits signal propagation across multiple nodes. Mapping the Ca2+ data onto the STED images of the morphology, showed that the majority of astrocytic Ca2+ signals were associated with single synapses suggesting that astrocytes are capable of engaging in synapse-specific communication.
Altogether, our study shines new light on the nanoscale organization of astrocytes in live brain tissue (organotypic and acute brain slices and in vivo), identifying astrocytic nodes as the elusive anatomical structure that may regulate neuronal communication at single ‘tripartite synapses’.
Reference:
Structural basis of astrocytic Ca2+ signals at tripartite synapses
Misa Arizono, V. V. G. Krishna Inavalli, Aude Panatier, Thomas Pfeiffer, Julie Angibaud, Florian Levet, Mirelle J. T. Ter Veer, Jillian Stobart, Luigi Bellocchio, Katsuhiko Mikoshiba, Giovanni Marsicano, Bruno Weber, Stéphane H. R. Oliet & U. Valentin Nägerl
Nature Communications volume 11, Article number: 1906 (2020)
https://www.nature.com/articles/s41467-020-15648-4
Contact chercheur:
Valentin Nägerl, IINS, valentin.nagerl@u-bordeaux.fr
Intestin et cerveau dans la maladie de Parkinson : une voie à double sens
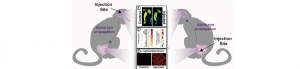
Plusieurs études ont récemment montré que la maladie de Parkinson pourrait trouver son origine dans l’intestin. En effet, des agrégats de la protéine alpha-synucléine, jouant un rôle clé dans le développement de la maladie, sont présents dans l’intestin. Une étude récente menée par une équipe franco-espagnole, chez des primates non-humains, montre que, non seulement la pathologie liée à l’alpha-synucléine peut être transportée de l’intestin vers le cerveau, mais aussi du cerveau à l’intestin. Cette étude ouvre de nouvelles perspectives sur notre compréhension du rôle de l’axe intestin/cerveau dans l’initiation et la propagation de la pathologie de la maladie de Parkinson.
La maladie de Parkinson est caractérisée, d’une part par la mort cellulaire d’une population neuronale spécifique, et d’autre part, par l’accumulation de la protéine alpha-synucléine dans ces cellules. L’idée que l’axe intestin-cerveau pourrait jouer un rôle dans l’initiation de la maladie a vu le jour en 2003 lorsqu’une équipe de neuro-anatomistes a découvert la présence d’inclusions d’alpha-synucléine dans le système nerveux entérique (i.e. intestin) de personnes décédées de la maladie de Parkinson. Cette découverte a permis de développer l’hypothèse selon laquelle la pathologie liée à l’accumulation d’alpha-synucléine se propagerait de l’intestin au cerveau. Cependant, l’origine intestinale de la MP n’a pas été prouvée chez les primates non humains et la possibilité que l’alpha-synucléine soit également transportée du cerveau à l’intestin est toujours à l’étude.
Des données récentes montrent que l’injection dans le cerveau d’agrégats d’alpha-synucléine provenant de cerveaux parkinsoniens peuvent initier et propager le processus neurodégénératif qui caractérise la maladie de Parkinson, chez la souris et le primate. L’étude entreprise ici chez les primates non-humains montre que l’injection d’agrégats d’alpha-synucléine provenant de cerveaux parkinsoniens, induit :
1- une neurodégénérescence, deux ans après l’injection, indépendant du site d’injection, cerveau ou bien intestin ;
2- des dépôts de la forme pathologique de la protéine alpha-synucléine, à la fois dans le système entérique et dans le cerveau. Il existe une corrélation entre le niveau élevé d’alpha-synucléine dans les neurones entériques et la neurodégénérescence progressive de la voie nigrostriatale ;
3- une accumulation d’une forme pathologique de l’alpha-synucléine, à la fois dans le cerveau et dans le système entérique, suite à une injection intracérébrale.
Ces résultats indiquent que la propagation de l’alpha-synucléine peut avoir lieu non seulement de l’intestin vers le cerveau, mais également du cerveau vers l’intestin. Comprendre comment la maladie se développe au fil du temps pourrait ouvrir la porte au développement de nouvelles approches thérapeutiques. Bien que d’autres expériences soient nécessaires, l’étude suggère également que la transmission de la pathologie de la α-synucléine ne passerait pas par le nerf vague comme cela avait été suggéré précédemment mais via un mécanisme systémique possible, dans lequel la circulation générale agirait comme une voie de transmission bidirectionnelle à longue distance de la α-synucléine endogène, renforçant le rôle prédictif de l’alpha-synucléine en tant que biomarqueur.
There is growing evidence that Parkinson’s disease (PD) may begin in the gut, with aggregates of the protein alpha-synuclein arising in the gut, playing a key role in the development of the disease. In experiments in non-human primates, a team of Spanish and French researchers say they have found additional evidence that brain alpha-synuclein can also travels down to the gut. This study offers a new invaluable primate data exploring the role of the gut-brain axis in the initiation and propagation of PD pathology.
Parkinson’s disease is characterized by the cell death of a specific neuronal population and by the buildup of a misfolded protein, called alpha-synuclein, in the cells of the brain. The research about the gut-brain axis emerged in 2003 when a neuroanatomists team spotted alpha-synuclein inclusions within the enteric nervous system of people who had died with PD. They proposed a staging scheme in which α-synuclein pathology spread from the gut to the brain. However, the intestinal origin of PD has not been proved in nonhuman primates and the bidirectional travel of alpha-synuclein is still under investigation. Recent data show that extracted α-synuclein aggregates of brains of dead patients have the ability to initiate and extend the neurodegenerative process that typifies Parkinson’s disease in mice and primates.
The study conducted in non-human primates shows that injection of extracted α-synuclein aggregates from PD patients have the ability to induce:
1- Two years after administration, injected monkeys displayed neurodegeneration regardless of the injection site, in the brain or in the gut.
2- Alpha-synuclein deposits of the pathological form of the protein was observed both in the enteric system and in the brain. We can observe a high α-synuclein level in enteric neurons correlated with the progressive destruction of the nigrostriatal pathway.
3- When the aggregates were injected into the brain, pathologic form of alpha-synuclein was observed both in the brain and in the enteric system and vice-versa.
These results indicate that both brain and gut injections of aggregates can induce α-synuclein pathology in the enteric system, demonstrating the bidirectional long-distance propagation of α-synuclein pathology between the brain and the gut in the non-human primate. Although further experiments are necessary, the study also suggests that the transmission of α-synuclein pathology does not go through the vagus nerve as it was previously suggested, but through a possible systemic mechanism, in which the general circulation would act as a route for long-distance bidirectional transmission of endogenous α-synuclein” explained Dr. Dehay, strengthening the predictive role of alpha-synuclein as a biomarker.
Pour en savoir plus:
Bidirectional gut-to-brain and brain-to-gut propagation of synucleinopathy in non-human primates. Arotcarena ML, Dovero S, Prigent A, Bourdenx M, Camus S, Porras G, Thiolat ML, Tasselli M, Aubert P, Kruse N, Mollenhauer B, Trigo-Damas I, Estrada C, Garcia-Carrillo N, Vaikath NN, El-Agnaf OMA, Herrero MT, Vila M, Obeso JA, Derkinderen P, Dehay B, Bezard E. Brain. 2020 May 1;143(5):1462-1475.
Contact chercheurs:
Benjamin Dehay, Ph.D
Erwan Bézard, Ph.D
Institut des Maladies Neurodégénératives (IMN), CNRS UMR 5293, Université de Bordeaux
Figure : Les injections cérébrales et intestinales d’une fraction enrichie d’agrégats humains d’alpha-synucléine induisent : 1 une dégénérescence nigro-striatale, 2 une pathologie alpha-synucléine dans le système nerveux central et 3 une pathologie alpha-synucléine dans le système entérique.
© Celine Perier
Expression enrichie des gènes de l’obésité dans des régions cérébrales clefs de l’addiction et de la récompense
L’obésité, qui est une maladie multifactorielle d’origine génétique et environnementale, est un enjeu majeur de santé publique dont la prévalence dans le monde a doublé pendant les 30 dernières années. Contrairement aux idées reçues, la composante génétique de l’obésité est très importante : en effet, les études réalisées à partir de familles, de jumeaux et d’enfants adoptés, ont permis d’évaluer une héritabilité élevée de la maladie, estimée autour de 70%.
Depuis 2007, les études d’association pangénomique (GWAS), basées sur l’utilisation de puces à ADN permettant de tester des centaines de milliers de variants fréquents dans la population générale, ont permis d’identifier plusieurs centaines de variants de l’ADN significativement associés à une augmentation de l’indice de masse corporelle ou du risque d’obésité. En d’autres termes, il a été démontré (et confirmé) que ces variants de l’ADN sont significativement plus fréquents chez les sujets obèses que chez les sujets normopondéraux. Cependant, malgré ce succès, les avancées physiopathologiques émanant de ces études GWAS ont été très décevantes. Ce constat est principalement lié au fait que ces variants de l’ADN ont un effet faible sur le risque de maladie. Par conséquent, il a été très complexe de d’évaluer leurs effets fonctionnels dans des modèles in vitro ou in vivo.
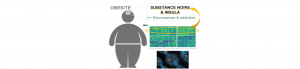
La grande majorité des variants identifiés par les études GWAS étant situés dans des zones intergéniques de l’ADN, nous avons au laboratoire analysé l’expression des gènes les plus proches des signaux d’association dans une grande variété de tissus humains (incluant plusieurs régions cérébrales), via une technologie permettant un comptage direct des ARN messagers sans aucune étape d’amplification évitant des biais. Nous avons trouvé que l’expression de ces gènes était très significativement enrichie dans la substance noire et l’insula, c’est-à-dire deux régions cérébrales impliquées dans les phénomènes de récompense et d’addiction. De plus, dans la cohorte issue de la population générale française D.E.S.I.R., nous avons démontré que les variants de l’ADN dont l’expression des gènes en proxy montrait le plus fort enrichissement dans la substance noire et l’insula, étaient au final les plus associés à une augmentation de l’indice de masse corporelle.
Par cette étude, nous montrons que la composante génétique humaine de l’obésité s’exprime avant tout dans des zones cérébrales ayant un rôle clef dans les phénomènes d’addiction et de récompense. Ce résultat se démarque très nettement des formes rares et sévères d’obésité monogénique, dont les gènes (par exemple MC4R, LEP, LEPR, POMC, SIM1, PCSK1, ADCY3, NTRK2, BDNF, SH2B1) jouent un rôle majeur dans la satiété et dans différentes voies neuro-endocrines, avec parfois un rôle dans le développement cérébral (comme SIM1). Nos résultats permettent d’envisager différemment la prise en charge des patients obèses : en effet, il faudrait inclure une prise en charge comportementale pour lutter contre l’addiction, et éviter les régimes restrictifs qui alimenteraient un sentiment de manque.
Référence :
Ndiaye FK, Huyvaert M, Ortalli A, Canouil M, Lecoeur C, Verbanck M, Lobbens S, Khamis A, Marselli L, Marchetti P, Kerr-Conte J, Pattou F, Marre M, Roussel R, Balkau B, Froguel P, Bonnefond A. The expression of genes in top obesity-associated loci is enriched in insula and substantia nigra brain regions involved in addiction and reward. Int J Obes (Lond). 2020 Feb;44(2):539-543. doi: 10.1038/s41366-019-0428-7. Epub 2019 Aug 6. PubMed PMID: 31388097; PubMed Central PMCID: PMC7002163.
Contact: Amélie Bonnefond
CNRS UMR 8199, European Genomic Institute for Diabetes (EGID)
Institut Pasteur de Lille, Université de Lille
Nouvelles pistes pour comprendre la résilience au trauma
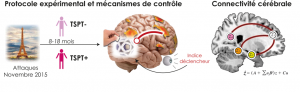
Les attentats de Paris et Saint-Denis, le 13 novembre 2015, ont laissé des marques durables, non seulement sur les survivants et leurs proches, mais aussi sur la société française dans son ensemble. Dans le cadre du programme transdisciplinaire 13-Novembre, une étude d’imagerie cérébrale en IRM intitulée Remember et menée à Caen, s’attèle à une question majeure qui intrigue les neuroscientifiques depuis des années : pourquoi certaines personnes ayant vécu un traumatisme souffrent-elles de stress post-traumatique, alors que d’autres, résilientes, ne développent jamais ce trouble ?
Le trouble de stress post-traumatique (TSPT) peut se développer chez certains individus ayant été confrontés à des événements traumatisants. Parmi les symptômes les plus caractéristiques, l’intrusion fréquente du souvenir des images, des odeurs et des sensations associées au traumatisme vécu, bouleversent la vie quotidienne et induisent une grande détresse. L’étude menée par les chercheurs Caenais, publiée dans la revue Science le 14 février 2020, permet de mieux comprendre l’origine des souvenirs intrusifs.
D’après les modèles traditionnels du TSPT, la persistance des souvenirs intrusifs douloureux s’expliquerait par un dysfonctionnement de la mémoire, et notamment de l’hippocampe, un peu à la manière d’un vinyle rayé rejouant en boucle les mêmes fragments de nos souvenirs. Par ailleurs, les tentatives par les patients de suppression et de contrôle de leurs souvenirs traumatiques ont longtemps été considérées comme un mécanisme inefficace et une stratégie négative, renforçant les intrusions et aggravant la situation des personnes souffrant de TSPT.
L’étude publiée dans Science remet en cause certaines de ces idées, et émet l’hypothèse que la résurgence intempestive des images et pensées intrusives serait liée à un dysfonctionnement des réseaux cérébraux impliqués dans le contrôle de la mémoire (pour reprendre l’image précédente, le bras de la platine vinyle contrôlant la lecture des souvenirs).
Afin de modéliser la résurgence des souvenirs intrusifs, sans les exposer à nouveau aux images choquantes des attentats, les chercheurs ont proposé un protocole de recherche s’appuyant sur la méthode Think/No-Think à 120 survivants des attaques de Paris, dont près de la moitié souffrait de TSPT. 73 personnes n’ayant pas été exposées aux attentats ont également pris part à l’étude. Cette méthode vise à créer des associations entre un mot indice et un objet du quotidien n’ayant rien à voir l’un avec l’autre (par exemple le mot « chaise » avec l’image d’un ballon), afin de reproduire la présence d’une intrusion lors de la confrontation avec le mot indice. Dans un second temps, la capacité des participants à chasser et supprimer l’image intrusive est mesurée par le biais de la connectivité cérébrale entre les régions de contrôle, situées dans le cortex préfrontal et les régions des souvenirs, telles que l’hippocampe.
Les résultats montrent que les participants souffrant de TSPT présentent une défaillance des mécanismes qui permettent de supprimer et de réguler l’activité des régions de la mémoire lors d’une intrusion (notamment l’activité de l’hippocampe). A l’inverse, cette capacité est largement préservée, voir supérieure, chez personnes résilientes. Ces résultats suggèrent que le mécanisme de suppression des souvenirs n’est pas intrinsèquement mauvais et à l’origine des intrusions comme on le croyait. En revanche, son dysfonctionnement l’est, ce qui conduit à sa surutilisation chez les TSPT.
Ces résultats soulignent que la persistance du souvenir traumatique n’est vraisemblablement pas uniquement liée à un dysfonctionnement de la mémoire, mais également à un dysfonctionnement de son contrôle. Reste à déterminer si ces difficultés de contrôle se sont instaurées après le traumatisme, ou étaient présentes avant, rendant l’individu plus vulnérable.
Ces résultats permettent également d’imaginer de nouvelles pistes de traitement. À l’heure actuelle, la plupart des thérapies existantes impliquent de se confronter au traumatisme, ce qui n’est pas toujours évident pour les patients. Proposer des interventions déconnectées des événements traumatiques, stimulant les mécanismes de contrôle identifiés dans cette étude, pourrait être un complément utile pour entraîner les patients à mettre en place des mécanismes de suppression plus efficaces.
Référence :
Mary A., Dayan J., Giovani Leone, Charlotte Postel, Florence Fraisse, Carine Malle, Thomas Vallée, Carine Klein-Peschanski, Fausto Viader, Vincent de la Sayette, Denis Peschanski, Francis Eustache, Pierre Gagnepain, « Resilience after trauma : the role of memory suppression ». Science 367, 756, 2020, DOI: 10.1126/science.aay8477
Contact chercheur :
INSERM-EPHE-UNICAEN U1077, « Neuropsychologie et Imagerie de la Mémoire Humaine » (NIMH),
GIP Cyceron, Caen
Connectivité altérée du réseau par défaut chez des adolescents présentant un Trouble de Stress Post-Traumatique
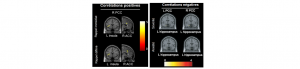
Le Trouble de Stress Post-Traumatique (TSPT) se caractérise par des symptômes d’intrusions, de reviviscence, d’évitement et d’hypervigilence. Ces symptômes pourraient être liés à un dysfonctionnement des régions clefs de réseaux neurocognitifs desservants les processus de référence à soi (réseau par défaut, RD), la détection de stimuli salients (réseau de la salience, RS) ou de dysfonctionnement cognitif (réseau central exécutif, RC). Les études en imagerie par résonance magnétique fonctionnelle (IRMf) au repos chez des adolescents ayant un TSPT sont rares et les résultats controversés, probablement dus à des différences dans la sévérité des symptômes. L’activité au repos a été enregistrée chez 14 adolescents présentant un TSPT sévère et 24 sujets témoins appariés en âge. Des analyses de connectivité en seed-based ont permis d’examiner la connectivité entre le RD et le reste du cerveau, y compris des régions d’autres réseaux (RS et RC). La relation entre ces réseaux et les symptômes (sévérité, anxiété et dépression), ainsi qu’avec la mémoire épisodique, ont également été examinés. Les analyses ont montré une hypoconnectivité au sein des régions du RD (entre le cortex cingulaire postérieur, PCC, et le cortex occipital) chez les patients par rapport aux témoins. De plus, la connectivité intra-RD (entre le PCC et l’hippocampe) étaient corrélée négativement avec les symptômes (sévérité et anxiété), alors qu’une hyperconnectivité (entre RD-RS et RD-RC) était corrélée positivement avec les scores de mémoire épisodique. Ces connectivités anormales entre réseaux cérébraux chez les adolescents présentant un TSPT corroborent les résultats chez l’adulte présentant un TSPT. L’hypoconnectivité intra-RD et la connectivité altérée avec les autres réseaux pourraient être à la base du rappel intrusif lié au trauma et du rappel épisodique autobiographique altéré dans le TSPT.
Référence: Viard et al. (2019) Altered default mode network connectivity in adolescents with post-traumatic stress disorder. Neuroimage: Clinical. 22:101731.
Contact chercheur : Armelle Viard
INSERM-EPHE-UNICAEN, U1077, Centre Cyceron, Caen
Un lien causal entre une diminution des taux d’acides gras polyinsaturés et des déficits motivationnels
Les pathologies psychiatriques, telles que la schizophrénie, les troubles bipolaires ou la dépression majeure sont classiquement considérées comme différentes d’un point de vue clinique du fait des catégories diagnostiques distinctes qui y sont associées. Cependant, ces pathologies présentent des symptômes communs et de plus en plus de données suggèrent l’existence de relations entre ces pathologies, qu’elles soient d’ordre génétique (polymorphismes génétiques communs) ou environnemental. Dans ce contexte, des données cliniques révèlent que ces pathologies s’accompagnent de modifications du métabolisme lipidique et en particulier d’une diminution « corps entier » des taux d’acide gras polyinsaturé (AGPI) n-3. Les AGPIs sont parmi les constituants majoritaires des membranes cellulaires au sein desquelles ils vont moduler les propriétés de la membrane et des protéines qui y sont associées et agir comme messagers secondaires.
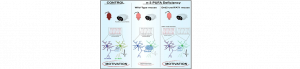
Dans une étude publiée dans le journal Cell Metabolism le 5 mars 2020, des chercheurs de l’INRAE et Université de Bordeaux montrent qu’une diminution du statut en AGPI n-3, en influant directement sur le système cérébral de la récompense, induit des déficits motivationnels, une dimension symptomatique commune à plusieurs pathologies psychiatriques. Plus précisément, ils montrent que la déficience développementale en AGPI n-3 conduit, à l’âge adulte, à une augmentation de l’inhibition dite « latérale » des neurones épineux moyens (medium spiny neurons ou MSN) qui expriment le récepteur à la dopamine D2 (D2R) sur les MSN qui expriment le récepteur D1 (D1R) dans le noyau accumbens. En utilisant un model transgénique unique, les auteurs ont pu établir un lien de causalité entre le statut en AGPI n-3 et les altérations neurobiologiques et comportementales. En effet, ils montrent que normaliser les taux d’AGPI pendant le développement périnatal, sélectivement dans les neurones qui expriment le D2R – mais pas ceux qui expriment le D1R -, est suffisant pour prévenir les altérations neurobiologiques et comportementales.
Ces résultats constituent la première démonstration de l’existence d’un lien causal entre des modifications de taux d’AGPI dans une sous-population neuronale spécifique et une altération comportementale. Ils mettent en évidence une vulnérabilité particulière des D2R-MSN – une population neuronale connue pour être dysfonctionnelle dans plusieurs pathologies – au statut en AGPI. Par ailleurs, cette étude suggère que la diminution des taux d’AGPI n-3 décrite dans plusieurs pathologies psychiatriques pourrait directement participer à l’étiologie de certains symptômes tels que l’avolition ou l’apathie. L’origine de cette réduction des AGPI n-3 chez le patient reste inconnue mais pourrait résulter de polymorphismes de certaines enzymes impliquées dans le métabolisme lipidique. Le statut en AGPI pourrait ainsi constituer un biomarqueur prédictif et spécifique de certains symptômes et endophénotypes psychiatriques.
Référence :
Causal Link between n-3 Polyunsaturated Fatty Acid Deficiency and Motivation Deficits
Cell metabolism, 2020, https://doi.org/10.1016/j.cmet.2020.02.012
Fabien Ducrocq,,* Roman Walle, Andrea Contini, Asma Oummadi, Baptiste Caraballo, Suzanne van der Veldt, Marie-Lou Boyer, Frank Aby, Tarson Tolentino-Cortez, Jean-Christophe Helbling, Lucy Martine, Stéphane Grégoire, Stéphanie Cabaret, Sylvie Vancassel, Sophie Layé, Jing Xuan Kang, Xavier Fioramonti, Olivier Berdeaux, Gabriel Barreda-Gomez, Elodie Masson, Guillaume Ferreira, David W.L. Ma, Clementine Bosch-Bouju, Veronique De Smedt-Peyrusse, and Pierre Trifilieff
Contact :
Les lipides nutritionnels contrôlent le système de la récompense
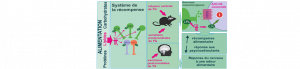
L’alimentation est sans doute essentielle à la survie mais est aussi source de plaisir. Depuis plusieurs années la littérature scientifique pointe des liens étroits entre alimentation trop riche, prise alimentaire compulsive et obésité.
Des scientifiques du CNRS et d’Université de Paris (Unité de Biologie Fonctionnelle et Adaptative 1,2) viennent de montrer comment les triglycérides, les lipides qui se retrouvent dans le sang après la digestion des graisses par notre intestin, agissent sur le cerveau, et notamment au niveau du « circuit de la récompense ». Publiés dans Cell Metabolism le 5 mars 2020, ces résultats apportent un éclairage nouveau sur le lien entre alimentation et dérèglements des comportements alimentaires.
A l’aide de plusieurs approches complémentaires et multi-échelles, ces travaux montrent que les triglycérides interagissent avec certains neurones du « circuit de la récompense » et diminuent leur excitabilité. Ces neurones portent un type spécifique de récepteur de la dopamine, le récepteur de type 2 (DRD2), et leur activité participe au renforcement des comportements de recherche de récompense. Les scientifiques ont d’ailleurs observé que la manipulation des taux de triglycérides dans le cerveau des souris modifie plusieurs comportements associés à la dopamine, comme le plaisir et la motivation à collecter de la nourriture.
De manière intéressante, ces mêmes neurones possèdent les outils moléculaires nécessaires à la détection et l’utilisation de ces lipides. En particulier, on trouve sur les neurones qui libèrent de la dopamine ou ceux qui, en aval reçoivent et répondent à la dopamine, une enzyme spécialisée dans le découpage des triglycérides en lipides plus simple et plus facilement utilisables par la cellule : la lipoprotéine lipase (LPL). Ces résultats laissent penser que les neurones du circuit de la récompense seraient donc en capacité de répondre aux triglycérides, comme ils répondent au neuromédiateur dopamine.
L’étude est complétée par la mesure de la réponse du cerveau à une odeur de nourriture dans des conditions de jeun ou après un repas. En collaboration avec nos collègues, nous avons montré que la réponse du cortex préfrontal, une des régions du circuit de la récompense, est directement corrélée à la quantité de triglycérides circulants après un repas. Plus les triglycérides sont élevés, plus la réponse du cortex préfrontal à une odeur alimentaire est atténuée, ce qui suggère que l’activité de structures cérébrales importantes du système de récompense peut être directement modifié par un nutriment lipidique.
Habituellement, les concentrations circulantes de triglycérides sont transitoires et fluctuent uniquement après un repas. Ce n’est pas le cas des patients obèses, chez lesquels on observe souvent une concentration trop élevée de triglycérides tout au long de la journée. On pourrait donc imaginer qu’un apport constant de « signaux » lipidiques finirait par perturber l’activité des neurones DRD2 et, par voie de conséquence, perturber la « récompense » associée à la nourriture, ce qui peut se traduire par une comportement alimentaire dérégulé.
Dans ce contexte, cette étude offre un nouveau cadre de lecture permettant potentiellement d’expliquer pourquoi l’accès de plus en plus répandu à des nourritures riches peut contribuer à l’établissement de troubles alimentaires de type compulsif et favoriser le développement de l’obésité.
Notes
1- Equipe COFFEE, http://bfa.univ-paris-diderot.fr/#
2- Ont également participé à ces travaux des chercheurs et chercheuses du Centre Interdisciplinaire de Recherche en Biologie (CNRS/Inserm/Collège de France), de l’Institut de Neurosciences Cognitives et Intégratives d’Aquitaine (CNRS/Université de Bordeaux) et du laboratoire Neurosciences Paris-Seine (CNRS/Inserm/Sorbonne Université) et, au niveau international, le Helmholtz Diabetes Center,de Munich, Yale University, University of California San Diego et la société Novo Nordisk.
Référence
Circulating triglycerides gate dopamine-associated behaviours through dopamine receptor type 2 (DRD2)-expressing neurons. Chloé Berland, Enrica Montalban, Elodie Perrin, Mathieu Di Miceli, Yuko Nakamura, Maud Martinat, Mary Sullivan, Xue S. Davis, Mohammad Ali Shenasa, Claire Martin, Stefania Tolu, Fabio Marti, Stephanie Caille, Julien Castel, Sylvie Perez, Casper Gravesen Salinas, Chloé Morel, Jacob Hecksher-Sørensen, Martine Cador, Xavier Fioramonti, Matthias H. Tschöp, Sophie Layé, Laurent Venance, Philippe Faure, Thomas S. Hnasko, Dana M. Small, Giuseppe Gangarossa et Serge Luquet. Cell Metabolism, le 5 mars 2020.
Contacts
LE METABOLISME DES ASTROCYTES S’INVITE DANS LA MALADIE D’ALZHEIMER
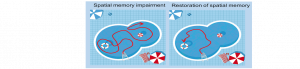
Des chercheurs du Laboratoire des maladies neurodégénératives (CNRS/CEA/Université Paris-Saclay) et du Neurocentre Magendie (Inserm/Université de Bordeaux) viennent de mettre en évidence le rôle déterminant que joue une voie métabolique dans les troubles de mémoire de la maladie d’Alzheimer. Leurs travaux, publiés le 3 mars 2020 dans Cell Metabolism, montrent également qu’un apport en acide aminé particulier, sous forme de complément alimentaire, restaure la mémoire spatiale atteinte de façon précoce chez des souris modèles de la maladie. Une piste prometteuse pour atténuer la perte de mémoire liée à Alzheimer.
Le cerveau consomme une grande partie de l’énergie disponible dans notre organisme. Son bon fonctionnement repose sur une étroite coopération entre les neurones et les cellules de leur environnement, en particulier les astrocytes. La phase précoce de la maladie d’Alzheimer est caractérisée par une réduction de ce métabolisme énergétique, mais on ignorait si ce déficit pouvait contribuer directement aux symptômes cognitifs de la maladie d’Alzheimer.
Cette étude collaborative a montré chez une souris modèle de la maladie d’Alzheimer que la diminution de la consommation de glucose par les astrocytes conduit à une réduction de la production de L-sérine, un acide aminé majoritairement produit par ces cellules dans le cerveau et dont la voie de biosynthèse est altérée chez les patients. La L-sérine est le précurseur de la D-sérine, connue pour stimuler les récepteurs NMDA, essentiels au bon fonctionnement du cerveau et à l’établissement de la mémoire. Dès lors, en produisant moins de L-sérine, les astrocytes sont à l’origine d’une diminution de l’activité de ces récepteurs, ce qui entraine une altération de la plasticité neuronale et des capacités de mémorisation associées. Les auteurs de l’étude ont également démontré que les fonctions de mémorisation des souris ont toutes été restaurées par un apport alimentaire en L-sérine.
L’identification du rôle de la L-sérine dans les troubles de la mémoire et l’efficacité expérimentale d’une supplémentation nutritionnelle ouvrent la voie à de nouvelles stratégies, complémentaires des thérapies médicamenteuses, pour lutter contre les symptômes précoces de la maladie d’Alzheimer et d’autres maladies présentant des altérations du métabolisme cérébral, comme les maladies de Parkinson ou de Huntington. La L-sérine étant disponible comme complément alimentaire, il convient de tester de façon rigoureuse cette molécule chez l’humain, à travers des essais cliniques encadrés.
Référence:
mpairment of Glycolysis-Derived l-Serine Production in Astrocytes Contributes to Cognitive Deficits in Alzheimer’s Disease. Le Douce J, Maugard M, Veran J, Matos M, Jégo P, Vigneron PA, Faivre E, Toussay X, Vandenberghe M, Balbastre Y, Piquet J, Guiot E, Tran NT, Taverna M, Marinesco S, Koyanagi A, Furuya S, Gaudin-Guérif M, Goutal S, Ghettas A, Pruvost A, Bemelmans AP, Gaillard MC, Cambon K, Stimmer L, Sazdovitch V, Duyckaerts C, Knott G, Hérard AS, Delzescaux T, Hantraye P, Brouillet E, Cauli B, Oliet SHR, Panatier A, Bonvento G. Cell Metab. 2020 Mar 3;31(3):503-517.e8. doi: 10.1016/j.cmet.2020.02.004.
Contact chercheurs:
Gilles Bonvento, Laboratoire des maladies neurodégénératives, CEA, CNRS, UMR 9199, Institut de Biologie François Jacob, MIRCen, Fontenay-aux-Roses.
Aude Panatier, Neurocentre Magendie, INSERM U1215, Université de Bordeaux, Bordeaux France.
Un engramme ocytocinergique pour apprendre et contrôler sa peur

Nos souvenirs définissent qui nous sommes, qui nous serons. L’idée d’une représentation physique de la mémoire remonte à il y a plus de 2000 ans. En 350 av. J.-C., Aristote théorisait que « le processus de stimulation sensorielle marque une sorte d’impression du percept, juste comme un sceau laisse son empreinte dans une cire chaude ». Cette idée a progressivement menée vers l’hypothèse selon laquelle des ensembles de cellules, organisés et sélectivement activés, forment les blocs de base de la trace mnésique, l’engramme. Cette hypothèse constitue aujourd’hui un champ majeur d’investigations, guidant l’étude des mécanismes cellulaires et moléculaires sous-jacents à l’encodage et la préservation de la mémoire. Le cerveau est l’organe le plus complexe qui soit, ayant évolué sur des centaines de millions d’années à partir de simples réseaux de neurones responsables de comportements simples, comme orchestrer la survie en évitant l’exposition au danger. La mémoire jouant un rôle clef dans la survie de l’individu, les constellations de cellules, interagissant entre elles pour former des engrammes, pourraient être évolutivement très anciennes. Pourtant, à ce jour, le dogme prédominant veut que la mémoire soit encodée dans l’hippocampe pour être ensuite stockée dans le cortex. Cette vision limitée ne prend que peu en considération les autres structures cérébrales, particulièrement celles évolutivement plus anciennes pouvant effectuer une réorganisation dynamique des circuits anatomiques et fonctionnels soutenant la formation et le stockage de la mémoire.
Lors d’une récente étude, dont les résultats sont publiés dans la revue Neuron (Hasan et al., 2019), l’équipe internationale animée et coordonnée par les Drs. Alexandre Charlet (France) et Valery Grinevich (Allemagne) démontre que des engrammes sont susceptibles de se former dans des structures comme l’hypothalamus. Pour ce faire, ils se sont intéressés aux neurones produisant l’ocytocine, un neuropeptide fortement impliqué dans la régulation des émotions, incluant la douleur et la peur. A l’aide d’une nouvelle méthode de ciblage génétique, permettant de cibler spécifiquement les neurones ocytocinergiques activés lors de l’une réaction de peur, les auteurs ont découvert la formation et l’intégration d’engrammes hypothalamiques dont la manipulation altère drastiquement l’expression et le souvenir d’une peur. En effet, l’activation optogénétique de ces cellules gomme entièrement l’expression de la peur; tandis que l’inhibition chémogénétique de cet engramme bloque son extinction, induisant sa persistance. Par ailleurs, ces neurones font preuve d’une étonnante plasticité, transitant d’une transmission lente médiée par le neuropeptide ocytocine vers une communication beaucoup plus rapide, via la sécrétion de glutamate. Cette découverte majeure marque un changement de paradigme, appelant à explorer plus avant l’existence et l’intégration des engrammes dans les différentes régions cérébrales. Comprendre les circuits anatomiques et fonctionnels sous-jacents d’une émotion telle que la peur, pourrait permettre l’émergence de nouvelles stratégies thérapeutiques, notamment quand la peur devient pathologique, comme dans le cas des troubles de stress post-traumatiques.
Référence : Hasan MT*, Althammer F*, Silva da Gouveia M*, Goyon S*, Eliava M, Lefevre A, Kerspern D, Schimmer J, Raftogianni A, Wahis J, Knobloch-Bollmann HS, Tang Y, Liu X, Jain A, Chavant V, Goumon Y, Weislogel J-M, Hurlemann R, Herpertz SC, Darbon P, Dogbevia GK, Bertocchi I, Larkum ME, Sprengel R, Bading H, Charlet A#, Grinevich V#. (2019). Fear Memory Engram and its Plasticity in the Hypothalamic Oxytocin System. Neuron, in press. #Corresponding and Co-senior authors; *Co-first authors
Contact chercheur :
CRCN CNRS, Institut des Neurosciences Cellulaires et Intégratives, CNRS UPR3212, Strasbourg